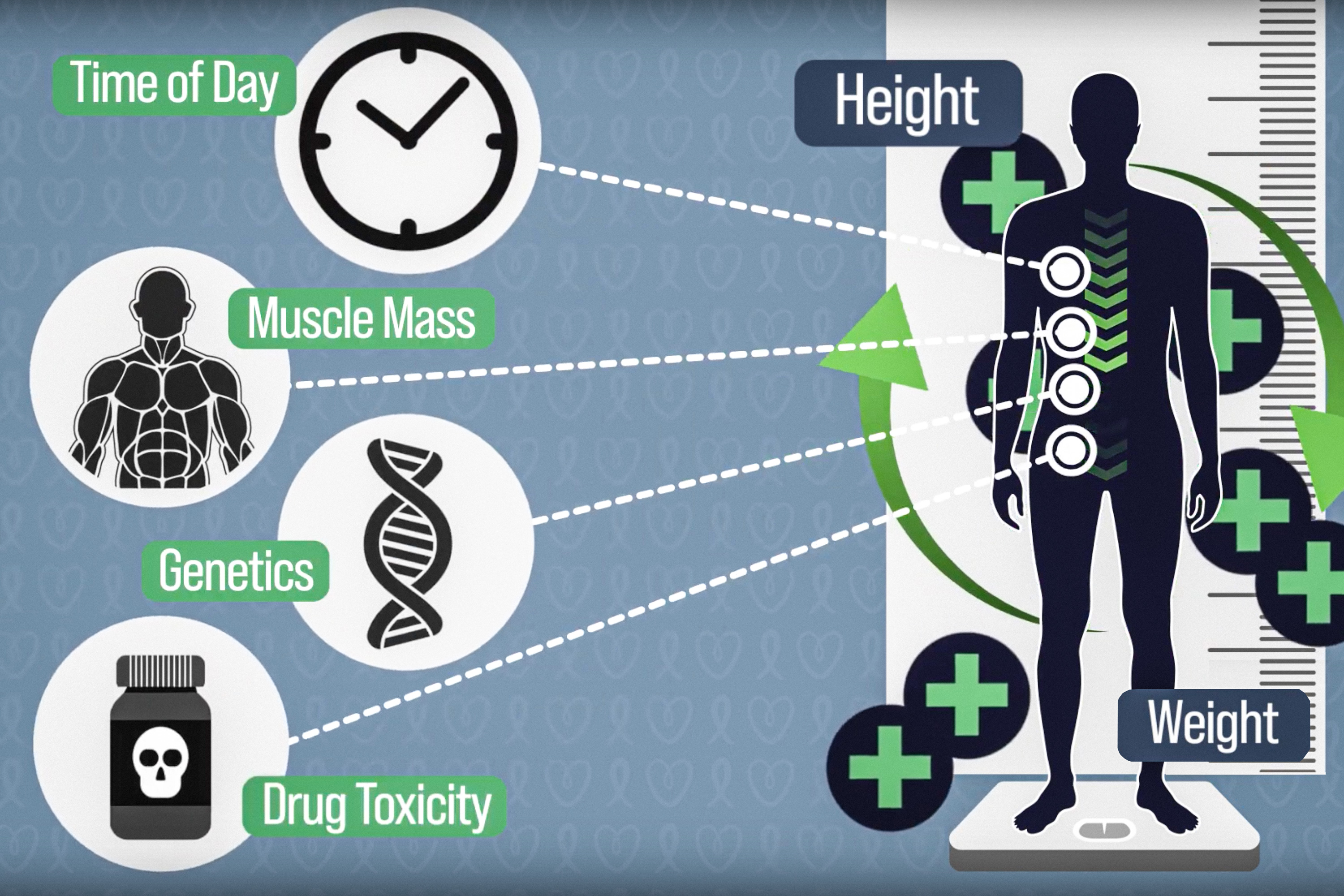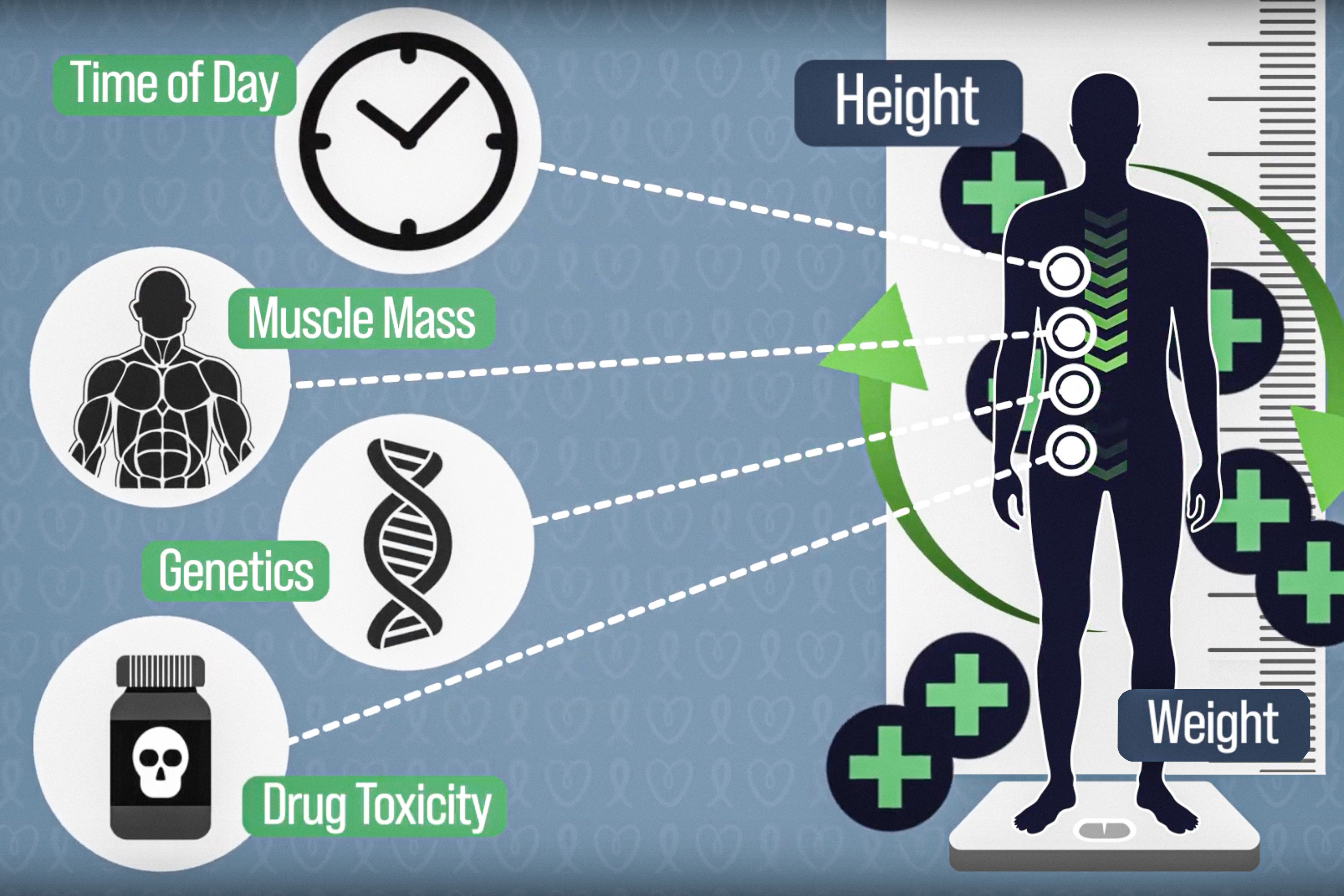
هنگامی که بیماران سرطانی تحت شیمی درمانی قرار می گیرند، دوز اکثر داروها بر اساس سطح بدن بیمار محاسبه می شود. این با وارد کردن قد و وزن بیمار به معادله ای که به سال 1916 برمی گردد و از داده های تنها 9 بیمار فرموله شده بود، محاسبه می شود.
این دوز ساده، عوامل دیگر را در نظر نمی گیرد و ممکن است منجر به دریافت بیش از حد یا خیلی کم دارو توسط بیماران شود. در نتیجه، برخی از بیماران احتمالاً سمیت قابل اجتناب یا سود ناکافی را از شیمی درمانی دریافت می کنند.
برای دقیقتر کردن دوز شیمیدرمانی، مهندسان MIT رویکرد جایگزینی را ارائه کردهاند که میتواند دوز را برای بیمار سفارشیسازی کند. سیستم آنها میزان دارو را در سیستم بیمار اندازه گیری می کند و این اندازه گیری ها به یک کنترل کننده وارد می شود که می تواند نرخ انفوزیون را متناسب با آن تنظیم کند.
این رویکرد میتواند به جبران تفاوتهای فارماکوکینتیک دارو ناشی از ترکیب بدن، ساختار ژنتیکی، سمیت ناشی از شیمیدرمانی در اندامهای متابولیزهکننده دارو، تداخل با سایر داروهای مصرفشده و غذاهای مصرفشده، و نوسانات شبانهروزی در آنزیمهای مسئول تخریب، کاهش داروهای شیمیدرمانی کمک کند. ، محققان می گویند.
جووانی تراورسو، دانشیار مهندسی مکانیک در MIT، متخصص گوارش در بریگهام میگوید: «با شناخت پیشرفتها در درک ما از نحوه متابولیسم داروها و استفاده از ابزارهای مهندسی برای تسهیل دوز شخصیسازی شده، معتقدیم که میتواند به تغییر ایمنی و اثربخشی بسیاری از داروها کمک کند. و بیمارستان زنان و نویسنده ارشد این مطالعه.
Lewis DeRidder، دانشجوی کارشناسی ارشد MIT، نویسنده اصلی این مقاله است کاغذکه امروز در مجله ظاهر می شود پزشکی.
نظارت مستمر
در این مطالعه، محققان بر روی دارویی به نام 5-fluorouracil تمرکز کردند که از جمله برای درمان سرطان کولورکتال استفاده می شود. این دارو معمولاً در طی 46 ساعت تزریق می شود و دوز با استفاده از فرمولی بر اساس قد و وزن بیمار تعیین می شود که سطح تقریبی سطح بدن را نشان می دهد.
با این حال، این رویکرد تفاوتهایی را در ترکیب بدن، که میتواند بر نحوه توزیع دارو در بدن یا تنوع ژنتیکی، که بر نحوه متابولیسم آن تأثیر میگذارد، تأثیر بگذارد، در نظر نمیگیرد. این تفاوت ها در صورت وجود بیش از حد دارو می تواند منجر به عوارض جانبی مضر شود. اگر دارو به اندازه کافی در گردش نباشد، ممکن است آنطور که انتظار می رود تومور را از بین نبرد.
“افرادی با سطح بدن یکسان می توانند قد و وزن بسیار متفاوتی داشته باشند، توده عضلانی یا ژنتیکی بسیار متفاوتی داشته باشند، اما تا زمانی که قد و وزن در نظر گرفته شده در این معادله سطح بدن یکسان را نشان دهد، دوز آنها یکسان است. DeRidder، کاندیدای دکترا در برنامه مهندسی پزشکی و فیزیک پزشکی در برنامه علوم و فناوری بهداشت هاروارد-MIT می گوید.
عامل دیگری که می تواند مقدار دارو را در جریان خون در هر زمان تغییر دهد، نوسانات شبانه روزی آنزیمی به نام دی هیدروپیریمیدین دهیدروژناز (DPD) است که 5-فلوئورواوراسیل را تجزیه می کند. بیان DPD، مانند بسیاری از آنزیم های دیگر در بدن، توسط یک ریتم شبانه روزی تنظیم می شود. بنابراین، تخریب 5-FU توسط DPD ثابت نیست، اما با توجه به زمان روز تغییر می کند. این ریتم های شبانه روزی می تواند منجر به نوسانات ده برابری در مقدار 5-فلوراوراسیل در جریان خون بیمار در طول انفوزیون شود.
با استفاده از سطح بدن برای محاسبه دوز شیمیدرمانی، میدانیم که دو نفر میتوانند سمیتهای متفاوتی نسبت به شیمیدرمانی 5-فلوئورواوراسیل داشته باشند. با نگاه کردن به یک بیمار، آنها می توانند چرخه های درمانی با حداقل سمیت داشته باشند و سپس یک چرخه سمیت بدی داشته باشند. چیزی در روش متابولیزه کردن شیمی درمانی این بیمار از یک سیکل به دوره دیگر تغییر کرد. داگلاس روبینسون، انکولوژیست بالینی در انستیتو سرطان دانا-فاربر و نویسنده مقاله گفت: دوز منسوخ شده ما نمی تواند این تغییر را ثبت کند و بیماران در نتیجه رنج می برند.
یکی از راههای مقابله با تغییر در فارماکوکینتیک شیمیدرمانی، راهبردی به نام نظارت بر داروی درمانی است که در آن بیمار در پایان یک چرخه درمان، نمونه خون میدهد. هنگامی که این نمونه از نظر غلظت دارو آنالیز شد، در صورت لزوم می توان دوز را در شروع چرخه بعدی تنظیم کرد (معمولاً دو هفته بعد برای 5-فلوئورواوراسیل). نشان داده شده است که این رویکرد منجر به نتایج بهتری برای بیماران می شود، اما به طور گسترده برای شیمی درمانی هایی مانند 5-fluorouracil استفاده نمی شود.
محققان MIT می خواستند نوع مشابهی از نظارت را توسعه دهند، اما به روشی که خودکار بود و امکان سفارشی سازی دارو در زمان واقعی را فراهم می کرد که می توانست به نتایج بهتری برای بیمار منجر شود. در سیستم “حلقه بسته” آنها، غلظت دارو را می توان به طور مداوم کنترل کرد و از این اطلاعات برای تنظیم خودکار میزان تزریق داروی شیمی درمانی و نگه داشتن دوز در محدوده هدف استفاده می شود. چنین سیستم حلقه بسته ای اجازه می دهد تا دوز دارو به گونه ای شخصی سازی شود که تغییرات ریتم شبانه روزی در سطح آنزیم های متابولیزه کننده دارو، و همچنین هرگونه تغییر در فارماکوکینتیک بیمار از آخرین درمان، مانند اندام ناشی از شیمی درمانی را در نظر بگیرد. سمیتی که داروها را متابولیزه می کند.
سیستم جدیدی که آنها طراحی کردند، معروف به CLAUDIA (تنظیم کننده تزریق خودکار دارو با حلقه بسته)، از تجهیزات تجاری موجود برای هر مرحله استفاده می کند. نمونه خون هر پنج دقیقه گرفته می شود و به سرعت برای تجزیه و تحلیل آماده می شود. غلظت 5- فلوئورواوراسیل در خون اندازه گیری و با محدوده هدف مقایسه می شود. تفاوت بین غلظت هدف و غلظت اندازهگیری شده به یک الگوریتم کنترل وارد میشود، که سپس نرخ تزریق را در صورت نیاز تنظیم میکند تا دوز را در محدوده غلظتهایی که دارو بین آنها موثر و غیرسمی است، حفظ کند.
DeRidder میگوید: «آنچه ما توسعه دادهایم سیستمی است که در آن میتوانید به طور مداوم غلظت دارو را اندازهگیری کنید و نرخ انفوزیون را متناسب با آن تنظیم کنید تا غلظت دارو را در پنجره درمانی نگه دارید.
راه اندازی سریع
در آزمایشهای حیوانی، محققان دریافتند که با استفاده از CLAUDIA، میتوانند مقدار داروی در حال گردش در بدن را در حدود 45 درصد مواقع در محدوده هدف نگه دارند. سطح دارو در حیواناتی که شیمی درمانی بدون CLAUDIA دریافت کردند، به طور متوسط تنها 13 درصد از مواقع در محدوده هدف باقی ماند. در این مطالعه، محققان هیچ آزمایشی در مورد اثربخشی سطوح دارو انجام ندادند، اما اعتقاد بر این است که حفظ غلظت در پنجره هدف منجر به نتایج بهتر و سمیت کمتری میشود.
CLAUDIA همچنین توانست دوز 5-fluorouracil را در محدوده هدف نگه دارد، حتی زمانی که محققان دارویی را تجویز کردند که آنزیم DPD را مهار می کند. در حیواناتی که این مهارکننده را بدون نظارت و اصلاح مستمر دریافت کردند، سطح 5-فلوراوراسیل تا 8 برابر افزایش یافت.
برای این نمایش، محققان هر مرحله از فرآیند را به صورت دستی و با استفاده از تجهیزات خارج از قفسه انجام دادند، اما اکنون قصد دارند روی خودکارسازی هر مرحله کار کنند تا نظارت و تنظیم دوز بدون دخالت انسان انجام شود.
برای اندازه گیری غلظت دارو، محققان از کروماتوگرافی مایع-طیف سنجی جرمی با کارایی بالا (HPLC-MS) استفاده کردند، تکنیکی که می تواند برای تشخیص تقریباً هر نوع دارویی سازگار باشد.
DeRidder میگوید: «ما آیندهای را تصور میکنیم که در آن قادر خواهیم بود از CLAUDIA برای هر دارویی که دارای خواص فارماکوکینتیک مناسب است و با HPLC-MS قابل تشخیص است، استفاده کنیم و در نتیجه امکان سفارشیسازی دوز برای بسیاری از داروهای مختلف را فراهم کنیم.
این تحقیق توسط برنامه کمک هزینه پژوهشی فارغ التحصیلان بنیاد ملی علوم، کمک هزینه تحصیلی MathWorks، استادی کارل ون تاسل MIT، دپارتمان مهندسی مکانیک MIT، و پروژه پل، مشارکت بین موسسه کخ برای تحقیقات سرطان یکپارچه در MIT و دانا-فاربر/مرکز سرطان هاروارد.
سایر نویسندگان مقاله عبارتند از: کایل ای. هار، آرون لوپز، جاش جنکینز، نینا فیتزجرالد، املین مک فرسون، نیورا فابیان، جاش موریموتو، ژاکلین ان. زکریا، کریستوفر ام. کولانجلو، هن وی هوانگ، ماکایا چیلکوا، نیکیل بی. لال، شریا اس. سرینیواسان، آلیسون ام. هیوارد، برایان ام. ولپین، دیوید ترامپر، تروی کواست و رابرت لنگر.